
SYBR Green 是一种经过验证的实时荧光定量PCR(qPCR)反应化学方法。它被认为简单、经济且准确。然而,这种方法并不像你想象的那样总是那么直接,对其进行适当优化有助于确保数据质量。正确设计和优化引物,并加入针对目标特异性的质量控制步骤,将有助于确保你的数据值得信赖。
SYBR Green 的工作原理是什么?
SYBR Green 是一种游离的荧光染料,能够与双链DNA结合,并在结合后增强荧光。在qPCR反应中,随着引物和DNA聚合酶复制模板链,SYBR Green 会与形成的双链DNA结合。qPCR仪器测量这种荧光,从而实现对原始样本中DNA含量的定量分析。
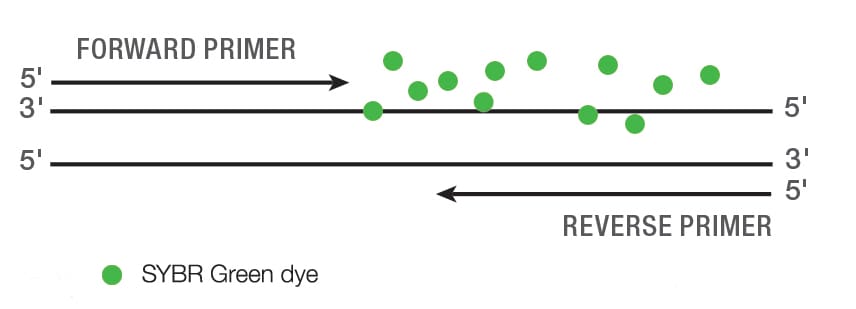
SYBR Green 的优势在于,由于它能与所有双链DNA结合,因此不需要特异性探针,这有助于降低成本。这是一种适用于大多数情况的方法,非常适合进行基因表达分析实验的研究人员,但这一优势也带来了一些缺点。由于其结合对象为所有双链DNA,意味着SYBR Green无法实现多重检测——也就是说,它不能在同一反应中同时分析多个特定靶标——并且还会对引物二聚体和非特异性扩增产生荧光响应。此外,不同的SYBR Green试剂盒对于主混合液中引物浓度的容忍度也不同。优化SYBR Green实验就是要找到减少这些信号噪音的方法,并确保荧光读数对应的是目标序列的扩增。这一系列确保结果可靠性的步骤从实验设计和优化阶段就开始了。
你的cDNA质量到底如何?
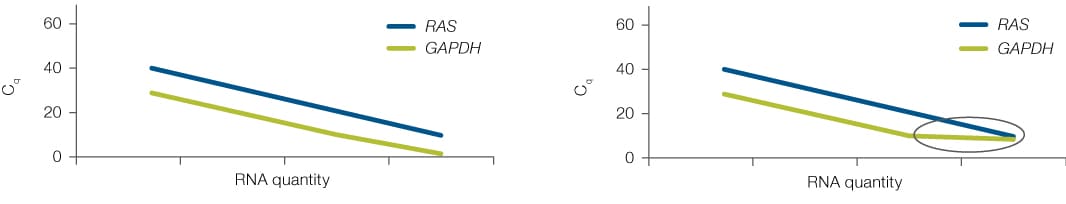
利用qPCR研究基因表达的关键步骤之一是合成cDNA。这是由RNA模板逆转录得到的DNA——在这里指的是你实际要研究的mRNA靶标。用于生成cDNA的酶——逆转录酶,有时会引入偏差,使得cDNA产量与样品中的RNA数量不总是成正比。这可以通过对已知浓度梯度稀释系列中的cDNA样品进行qPCR扩增目标基因和内源性对照,然后绘制标准曲线来检测。通过比较目标检测和内源性对照检测所得的qPCR标准曲线,可以确定哪些RNA含量会导致逆转录偏差。如需了解更多信息,请观看我们的:Taq Talk 视频,内容关于如何优化 SYBR Green 实验。
熔解曲线分析
SYBR Green染料会非特异性地结合到双链DNA上,因此检查SYBR Green qPCR反应是否只扩增了单一目标且没有引物二聚体形成的最佳方法是熔解曲线分析。熔解曲线分析在qPCR运行结束后进行,用于验证在实验过程中检测到的荧光是否来自单一扩增产物。由于SYBR Green作为荧光染料具有非特异性,熔解曲线分析成为确认目标特异性扩增发生的极少数方法之一。如果产生的部分荧光是由于引物二聚体或非特异性扩增造成的,那么对目标的相对定量就值得怀疑。因此,在建立新的SYBR Green检测时,始终将熔解曲线分析作为质量控制步骤,以帮助确认目标特异性。
在熔解曲线分析过程中,温度会从约60°C逐步升高至约95°C,使DNA变性。在只有单一扩增产物的qPCR反应体系中,随着DNA变性,荧光会平滑下降,直到最后全部变性,剩余荧光急剧降至背景值。下降过程中的中点温度即为该PCR产物的推定熔解温度。在分析软件中选择导数熔解曲线视图,可以将下降过程转换为一个峰值。
观察到单一峰值表明(但并不证明)只扩增了一个产物。这可以通过琼脂糖凝胶电泳分析PCR扩增产物来进一步确认。如果在凝胶上观察到单一条带,则进一步证明只扩增了一个产物。
如果观察到多个峰、主峰上的肩部、异常宽或不对称的峰,则提示可能形成了引物二聚体或发生了非特异性扩增或其他异常情况。
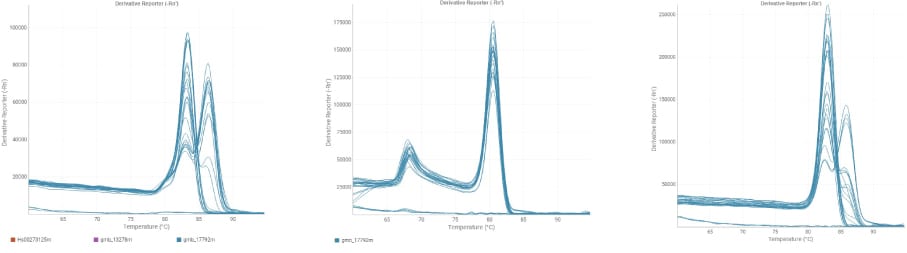
多重峰值主要有两个来源:非特异性扩增和引物二聚体形成。
- 非特异性复制是指引物与非目标序列结合并促进其扩增。提高引物特异性可以帮助防止这种非特异性扩增,使引物仅与所需目标结合。
- 引物二聚体形成是指引物之间相互结合。当引物结构足够对称时,它们可能自我结合或与自身反向引物结合。有时,通过降低反应中的引物浓度或提高退火温度即可减少引物二聚体形成,但有时需要重新设计引物以降低其发生概率。
一些曲线形状,包括不对称或非常宽的峰值,表明存在更为异常的问题,这类问题更难诊断。尤其是看起来异常的熔解曲线峰值,可能需要重新运行实验、重新设计实验或进行仪器诊断。如需了解更多关于熔解曲线分析的信息,请参考我们的Taq Talk节目关于如何执行这一重要质量控制步骤,以及阅读我们的白皮书,了解如何优化SYBR Green qPCR检测方法。
理解SYBR Green检测方法的工作原理,并设计能够应对其基本特性的实验和方案,有助于确保每一次实验都尽可能成功。始终使用熔解曲线分析QC测试新的SYBR Green检测方法,以帮助确认靶标特异性,从而让您可以信赖数据的准确性。
了解更多信息
qPCR数字手册2.0版:探索qPCR最佳实践、基本原理及故障排除技巧。
浏览Applied Biosystems Taq Talk视频系列全集:作为qPCR领域的资深专家,我们为您解答最常见的qPCR问题与挑战。
仅供科研使用。不得用于诊断程序。




发表回复