Search
Thermo Scientific Chemicals
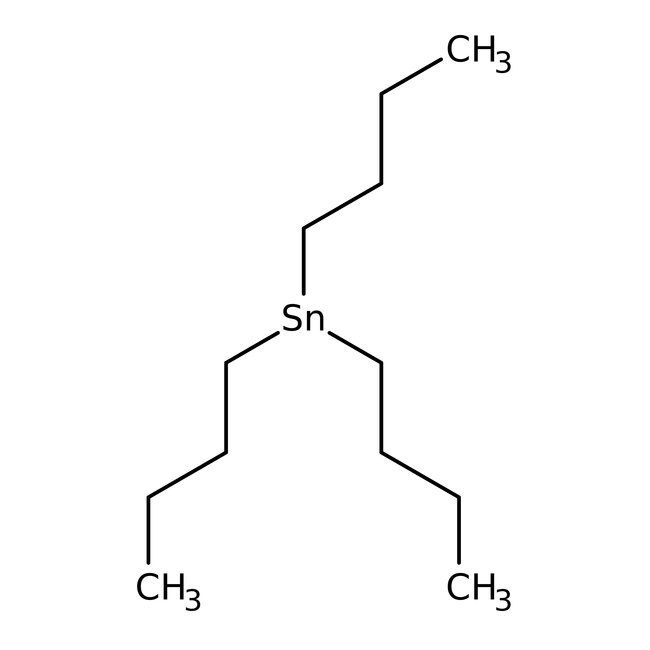
Hydrure de tri-n-butylétain, 97 %, Thermo Scientific Chemicals
CAS: 688-73-3 | C12H27Sn | 290.058 g/mol
Référence A13298.30
également connu sous le numéro A13298-30
Prix (EUR)
444,00
Each
Quantité:
250 g
Prix (EUR)
444,00
Each
Identifiants chimiques
CAS688-73-3
IUPAC Nametributylstannyl
Molecular FormulaC12H27Sn
InChI KeyPIILXFBHQILWPS-UHFFFAOYSA-N
SMILESCCCC[Sn](CCCC)CCCC
Voir plus
Spécifications Fiche de spécifications
Fiche de spécifications
FormLiquid
Refractive Index1.4705-1.4755 @ 20?C
CommentMay form slight precipitate on storage. May develop pressure.
Appearance (Color)Clear or slightly hazy, colorless
Assay (GC)≥96.0%
Voir plus
Tri-n-butyltin hydride is used as a radical reagent in reductive cleavage, radical dehalogenation and intramolecular radical cyclization. It also promotes intramolecular cyclization leading to isoxazolo-benzaulene ring system. Further, it acts as a reducing agent for the conversion of alkyl halides to hydrocarbons. In addition to this, it is used in a veterinary anthelmintic for poultry and an intermediate to make other butyltin compounds.
This Thermo Scientific Chemicals brand product was originally part of the Alfa Aesar product portfolio. Some documentation and label information may refer to the legacy brand. The original Alfa Aesar product / item code or SKU reference has not changed as a part of the brand transition to Thermo Scientific Chemicals.
Applications
L’hydrure de tri-n-butylétain est utilisé comme réactif radicalaire dans le clivage réductif, la déshalogénation radicalaire et la cyclisation des radicaux intramoléculaires. Il favorise également la cyclisation intramoléculaire conduisant au système de composés cycliques d’isoxazolo-benzaulène. De plus, il agit comme agent réducteur pour la conversion des halogénures d’alkyle en hydrocarbures. En outre, il est utilisé dans un anthelmintique vétérinaire pour la volaille et dans un intermédiaire pour fabriquer d’autres composés de butylétain
Solubilité
Immiscible avec l’eau.
Remarques
Sensible à l’air et à l’humidité. Stocker dans un endroit frais. Incompatible avec les agents oxydants et les acides minéraux.
L’hydrure de tri-n-butylétain est utilisé comme réactif radicalaire dans le clivage réductif, la déshalogénation radicalaire et la cyclisation des radicaux intramoléculaires. Il favorise également la cyclisation intramoléculaire conduisant au système de composés cycliques d’isoxazolo-benzaulène. De plus, il agit comme agent réducteur pour la conversion des halogénures d’alkyle en hydrocarbures. En outre, il est utilisé dans un anthelmintique vétérinaire pour la volaille et dans un intermédiaire pour fabriquer d’autres composés de butylétain
Solubilité
Immiscible avec l’eau.
Remarques
Sensible à l’air et à l’humidité. Stocker dans un endroit frais. Incompatible avec les agents oxydants et les acides minéraux.
RUO – Research Use Only
Références générales :
- Agent réducteur et source de radicaux tributylétain. Largement utilisé pour la réduction sélective des halogénures d’alkyle en alcanes par un mécanisme de chaîne radicalaire. La réaction est tolérante à une large gamme de fonctions, y compris OH et NH, contrairement aux réactifs d’hydrure métallique polaire. Pour les analyses, voir : Synthesis, 499 (1970) ; 665 (1987). Pour une brève caractéristique des utilisations de ce réactif en synthèse, voir : Synlett 173 , (2007 ). Utilisation dans la synthèse des sucres désoxy via un réarrangement réducteur des bromures de glycosyle, voir : Org. Synthé. Coll., 8, 583 (1993). La cyclisation du radical alkyle formé initialement à une double liaison correctement positionnée peut se produire. La formation de cycles à 5 membres est fortement favorisée et la fermeture d’un cycle sur un cycle existant donne le produit à fusion cis. Voir, par ex : J. Am. Chem. Soc., 108, 5893 (1986) :
- Le couplage intermoléculaire avec des alcènes déficients en électrons est également efficace : Angew. Chem. Int. Ed., 23, 69 (1984) ; Org. Synthé. Coll., 8, 148 (1993). Bilan Synthèse 417 (1988).
- Les alcools secondaires peuvent être désoxygénés par réduction de leurs dérivés xanthates : J. Chem. Soc., Perkin 1, 1574 (1975) ; Org. Synthé. Coll., 7, 139 (1990), ce qui évite les réarrangements rencontrés avec les méthodes basées sur la carbocation.
- Le TBTH clive également d’autres liaisons C-hétéroatome, contrôlées par la stabilité du radical résultant : Les groupes nitro des centres tertiaires sont facilement clivés : Synthèse 693 (1986). Les azides sont facilement réduits en amines : Synlett 342 , (1991 ). les liaisons C-S et C-Se sont également clivées. J. Am. Chem. Soc., 104, 2046 (1982) ; 112, 4008 (1990) ; J. Org. Chem., 49, 5206 (1984) ; 54, 1234 (1989).
- Les dialdéhyde et les céto-aldéhydes subissent un couplage pinacol intramoléculaire de radicaux libres pour donner des diols cycliques : J. Am. Chem. Soc., 117, 7283 (1995) ; J. Org. Chem, 63, 6357 (1998).