Search
Thermo Scientific Chemicals
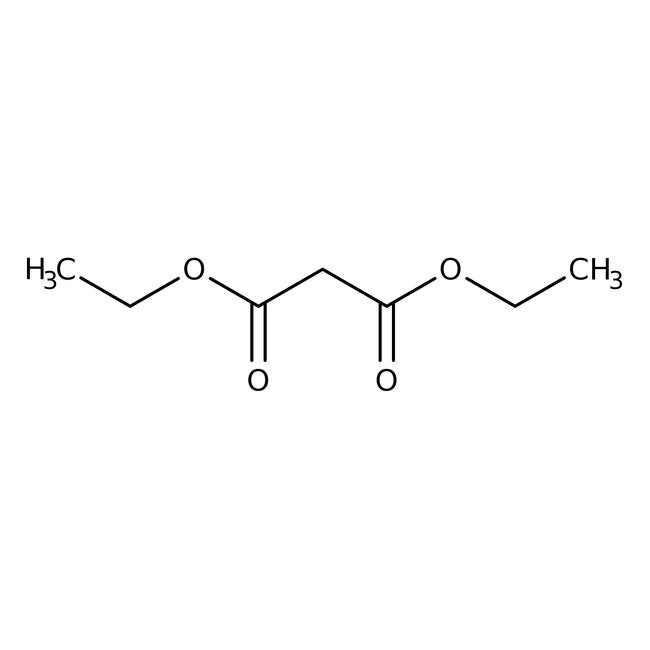
Malonate de diéthyle, 99 %, Thermo Scientific Chemicals
CAS: 105-53-3 | C7H12O4 | 160.169 g/mol
Référence A15468.0E
également connu sous le numéro A15468-0E
Prix (EUR)
96,65
Online Exclusive
107,00Économisez 10,35 (10%)
Each
Quantité:
2500 g
Prix (EUR)
96,65
Online Exclusive
107,00Économisez 10,35 (10%)
Each
Identifiants chimiques
CAS105-53-3
IUPAC Name1,3-diethyl propanedioate
Molecular FormulaC7H12O4
InChI KeyIYXGSMUGOJNHAZ-UHFFFAOYSA-N
SMILESCCOC(=O)CC(=O)OCC
Voir plus
Spécifications Fiche de spécifications
Fiche de spécifications
Assay (GC)≥98.5%
Water Content (Karl Fischer Titration)≤0.5%
Appearance (Color)Clear colorless
Refractive Index1.4125-1.4155 @ 20?C
Identification (FTIR)Conforms
Voir plus
Diethyl malonate is used in organic synthesis for the preparation of alpha-aryl malonates, mono-substituted and di-substituted acetic acid, barbiturates and artificial flavorings. It is also involved in the synthesis of pharmaceuticals like chloroquine, butazolidin and barbital. It acts as intermediate in the synthesis of vitamin B1, vitamin B6, non-steroidal anti-inflammatory agents agrochemicals and perfumes. In Knoevenagel condensation reaction, it reacts with benzaldehyde to get diethyl benzylidenemalonate.
This Thermo Scientific Chemicals brand product was originally part of the Alfa Aesar product portfolio. Some documentation and label information may refer to the legacy brand. The original Alfa Aesar product / item code or SKU reference has not changed as a part of the brand transition to Thermo Scientific Chemicals.
Applications
Le malonate de diéthyle est utilisé en synthèse organique pour la préparation de malonates d’alpha-aryle, d’acide acétique mono-substitué et di-substitué, de barbituriques et d’arômes artificiels. Il participe également à la synthèse de produits pharmaceutiques tels que la chloroquine, le butazolidine et le barbital. Il agit comme intermédiaire dans la synthèse de la vitamine B1, de la vitamine B6, des agents anti-inflammatoires agrochimiques non stéroïdiens et des parfums. Dans la réaction de condensation de Knoevenagel, il réagit avec le benzaldéhyde pour obtenir le benzylidénemalonate de diéthyle.
Solubilité
Miscible à l’alcool éthylique, à l’éther, au chloroforme et au benzène. Légèrement miscible avec de l’eau.
Remarques
Incompatible avec les acides, les bases, les agents oxydants et les agents réducteurs.
Le malonate de diéthyle est utilisé en synthèse organique pour la préparation de malonates d’alpha-aryle, d’acide acétique mono-substitué et di-substitué, de barbituriques et d’arômes artificiels. Il participe également à la synthèse de produits pharmaceutiques tels que la chloroquine, le butazolidine et le barbital. Il agit comme intermédiaire dans la synthèse de la vitamine B1, de la vitamine B6, des agents anti-inflammatoires agrochimiques non stéroïdiens et des parfums. Dans la réaction de condensation de Knoevenagel, il réagit avec le benzaldéhyde pour obtenir le benzylidénemalonate de diéthyle.
Solubilité
Miscible à l’alcool éthylique, à l’éther, au chloroforme et au benzène. Légèrement miscible avec de l’eau.
Remarques
Incompatible avec les acides, les bases, les agents oxydants et les agents réducteurs.
RUO – Research Use Only
Références générales :
- Pour la monoalkylation par transfert de phase du groupe de méthylène actif, voir par exemple (18-couronne-6) : Synthèse, 37 (1977) ; et (BTEAC) : Org. Prep. Proced. Int., 26, 469 (1994). L’alkylation du transfert de phase solide-liquide a été favorisée par l’irradiation aux micro-ondes : Synthé. Commun, 25,1761 , (1995 ). La dialkylation peut également se produire en présence de BTEAC : Synthesis, 54 (1985) ; Org. Synthé. Coll., 7, 411 (1990), pour donner des dérivés du cyclopropane. L’alkylation stéréosélective a été obtenue dans des conditions particulièrement douces avec des mésylates d’alkyle secondaires en présence de fluorure de césium, 12885 dans le DMF ; une inversion complète se produit au niveau du carbone alkyle secondaire : J. Org. Chem., 60, 2627 (1995) ; voir aussi : Synlett 499 , (1998 ).
- Les substituants peuvent également être introduits par l’ajout de Michael ; voir par exemple : Org. Synthé. Coll., 8, 467 (1993).
- L’arylation se produit avec les bromures d’aryle en présence de CuI : Gazz. Chim. Ital., 122, 511 (1992).
- L’acylation en C des esters maloniques est normalement effectuée par réaction du dérivé Mg avec un chlorure d’acide. Une méthode pratique utilisant une combinaison de MgCl2 et de triéthylamine a été introduite par Rathke : J. Org. Chem., 50, 2622 (1985) ; voir aussi Triéthyl-amine, A12646 pour une analyse de ce système :
- Un certain nombre de procédures ont été conçues pour la conversion directe d’esters maloniques en esters acétiques (décarboalkoxylation), en une seule étape dont le chauffage dans le DMSO humide est peut-être le plus simple : J. Org. Chem, 43, 138 (1978). Voir aussi 1,4-Diazabicyclo[2.2.2]octane, A14003.
- Comparez également Diméthyl-malonate, A11007, Di-tert-butyl-malonate, A12774, dibenzyl-malonate, A10844 et isopropyl-malonate d’idène, A15603.