Search
Thermo Scientific Chemicals
N-acétyl-DL-tryptophane, 99 %, Thermo Scientific Chemicals
CAS: 87-32-1 | C13H14N2O3 | 246.27 g/mol
Référence A17562.14
également connu sous le numéro A17562-14
Prix (EUR)
32,30
Online Exclusive
38,00Économisez 5,70 (15%)
Each
Quantité:
25 g
Prix (EUR)
32,30
Online Exclusive
38,00Économisez 5,70 (15%)
Each
Identifiants chimiques
CAS87-32-1
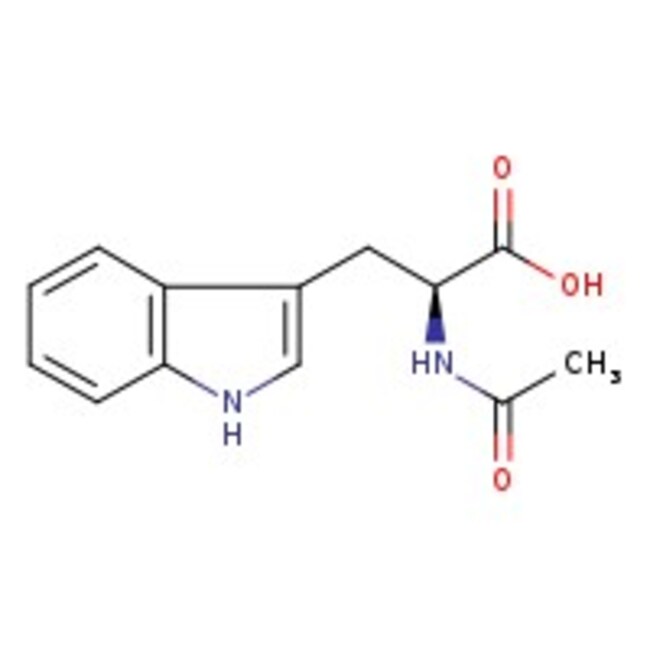
IUPAC Name2-acetamido-3-(1H-indol-3-yl)propanoic acid
Molecular FormulaC13H14N2O3
InChI KeyDZTHIGRZJZPRDV-UHFFFAOYSA-N
SMILESCC(=O)NC(CC1=CNC2=CC=CC=C12)C(O)=O
Voir plus
Spécifications Fiche de spécifications
Fiche de spécifications
Appearance (Color)White to pale cream
FormCrystals or powder or crystalline powder
Assay (Aqueous acid-base Titration)≥98.0 to ≤102.0%
Assay (HPLC)≥98.0%
N-Acetyl-DL-tryptophan is produced via chemical synthesis using the standard amino acid, tryptophan. It can be used in downstream applications of biopharmaceutical production as a transfer agent or stabilizer.
This Thermo Scientific Chemicals brand product was originally part of the Alfa Aesar product portfolio. Some documentation and label information may refer to the legacy brand. The original Alfa Aesar product / item code or SKU reference has not changed as a part of the brand transition to Thermo Scientific Chemicals.
Applications
Le N-acétyl-DL-tryptophane est produit par synthèse chimique à l’aide de l’acide aminé standard, le tryptophane. Il peut être utilisé dans les applications en aval de la production biopharmaceutique comme agent de transfert ou stabilisateur.
Solubilité
Soluble dans l’hydroxyde de sodium 1N, l’eau et le méthanol.
Remarques
Garder le récipient hermétiquement fermé. Conserver à l’abri des oxydants.
Le N-acétyl-DL-tryptophane est produit par synthèse chimique à l’aide de l’acide aminé standard, le tryptophane. Il peut être utilisé dans les applications en aval de la production biopharmaceutique comme agent de transfert ou stabilisateur.
Solubilité
Soluble dans l’hydroxyde de sodium 1N, l’eau et le méthanol.
Remarques
Garder le récipient hermétiquement fermé. Conserver à l’abri des oxydants.
RUO – Research Use Only
Références générales :
- Harold Edelhoch. Spectroscopic Determination of Tryptophan and Tyrosine in Proteins. Biochemistry. 1967, 6, (7), 1948-1954.
- Ferenc J. Kezdy.; Gerald E. Clement.; Myron L. Bender. The Observation of Acyl-Enzyme Intermediates in the α-Chymotrypsin-Catalyzed Reactions of N-Acetyl-L-tryptophan Derivatives at Low pH. J. Am. Chem. Soc. 1964, 86, (18), 3690-3696.