Search
Thermo Scientific Chemicals
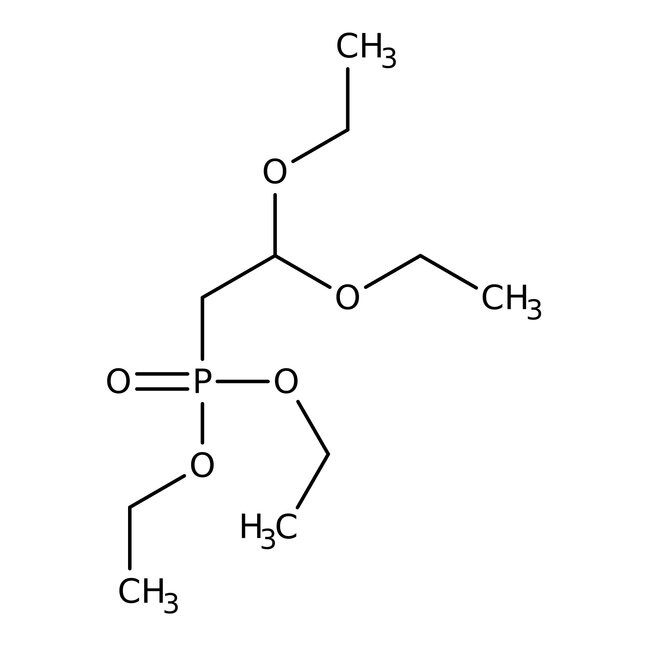
Diethyl2,2 -Diethoxyethylphosphonat, 96 %, Thermo Scientific Chemicals
CAS: 7598-61-0 | C10H23O5P | 254.263 g/mol
Katalognummer A12461.30
auch als A12461-30 bezeichnet
Preis (EUR)
995,00
Each
Menge:
250 g
Preis (EUR)
995,00
Each
Chemikalien-Kennzeichnungen
CAS7598-61-0
IUPAC Namediethyl (2,2-diethoxyethyl)phosphonate
Molecular FormulaC10H23O5P
InChI KeyLUQYELQXRPNKRY-UHFFFAOYSA-N
SMILESCCOC(CP(=O)(OCC)OCC)OCC
Mehr anzeigen
Specifications Datenblatt
Datenblatt
Appearance (Color)Clear colorless
Refractive Index1.4240-1.4300 @ 20?C
Assay (GC)≥95.0%
FormLiquid
Diethyl 2,2-diethoxyethylphosphonate is used reactant for synthesis of α,β-alkenal derivatives by two-carbon homologation, lower rim-phosphonylated rexorcinol calix[4]arenes by condensation reactions, α-Phosphovinyl radicals via a radical trapping sequence, inhibitors of reverse transcriptase via 1,3-dipolar cycloadditions and for Friedel-Crafts reactions.
This Thermo Scientific Chemicals brand product was originally part of the Alfa Aesar product portfolio. Some documentation and label information may refer to the legacy brand. The original Alfa Aesar product / item code or SKU reference has not changed as a part of the brand transition to Thermo Scientific Chemicals.
Anwendungen
Diethyl-2,2-Diethoxyethylphosphonat wird verwendet zur Synthese von α,β-Alkenderivaten durch Zwei-Kohlenstoff-Homologation, niederrangige-phosphonylierte Rexorcinol-calix[4]Arene durch Kondensationsreaktionen, α-Phosphovinyl-Radikale über eine Radikalen-Trapping-Sequenz, Inhibitoren der reversen Transkriptase über 1,3-dipolare Cycloadditionen und für Friedel-Crafts-Reaktionen.
Löslichkeit
Löslich in Chloroform und Dichlormethan. Nicht mischbar oder schwer in Wasser mischbar.
Hinweise
Halten Sie den Behälter dicht verschlossen. Es ist von Natur aus hygroskopisch. Sie ist empfindlich gegenüber Feuchtigkeit. Unter trockenem Inertgas lagern. Vor Feuchtigkeit und Wasser schützen.
Diethyl-2,2-Diethoxyethylphosphonat wird verwendet zur Synthese von α,β-Alkenderivaten durch Zwei-Kohlenstoff-Homologation, niederrangige-phosphonylierte Rexorcinol-calix[4]Arene durch Kondensationsreaktionen, α-Phosphovinyl-Radikale über eine Radikalen-Trapping-Sequenz, Inhibitoren der reversen Transkriptase über 1,3-dipolare Cycloadditionen und für Friedel-Crafts-Reaktionen.
Löslichkeit
Löslich in Chloroform und Dichlormethan. Nicht mischbar oder schwer in Wasser mischbar.
Hinweise
Halten Sie den Behälter dicht verschlossen. Es ist von Natur aus hygroskopisch. Sie ist empfindlich gegenüber Feuchtigkeit. Unter trockenem Inertgas lagern. Vor Feuchtigkeit und Wasser schützen.
RUO – Research Use Only
Allgemeine Referenzen:
- Richard J Petroski; Karl Vermillion; Allard A Cossé: Two-carbon homologation of aldehydes and ketones to α,β-unsaturated aldehydes. Molecules. 2011, 16 (6), 5062-5078.
- Ugo Chiacchio; Emanuela Balestrieri; Beatrice Macchi; Daniela Iannazzo; Anna Piperno; Antonio Rescifina; Roberto Romeo; Monica Saglimbeni; M Teresa Sciortino; Vincenza Valveri; Antonio Mastino; Giovanni Romeo: Synthesis of phosphonated carbocyclic 2'-oxa-3'-aza-nucleosides: novel inhibitors of reverse transcriptase. Journal of Medicinal Chemistry. 2005, 48 (5), 1389-1394.
- Wadsworth-Emmons-Olefination mit Aldehyden führt zu ɑß-enalen: Bull. Chem. Soc. Jpn., 30, 1498 (1962). Diese Reaktion schlägt für Ketone fehl, da das Ylid EtO- verliert. Dies kann durch die vorherige Umwandlung des Acetals in das entsprechende Cyclohexyl-Enamin vermieden werden: Org. Synth. Coll., 6, 448 (1988), gefolgt von der Reaktion mit dem Keton: Org. Synth. Coll., 6, 358 (1988):