Search
Zitierungen und Referenzen (8)
Invitrogen™
Click-iT™ Plus TUNEL-Assay-Kits für In Situ Apoptose-Detektion
Nachweis von Apoptose in Zellen und Gewebeproben mit Click-iT Plus TUNEL Assay-Kits, die eine einfache Farbstoffeinarbeitung und ein Multiplexing mit GFP und RFP ermöglichen.
| Katalognummer | Farbe | Marker oder Farbstoff |
|---|---|---|
| C10619 | Tiefrot | Alexa Fluor™ 647 |
| C10617 | Grün | Alexa Fluor™ 488 |
| C10618 | Rot | Alexa Fluor™ 594 |
Katalognummer C10619
Preis (EUR)
720,65
Online Exclusive
792,00Ersparnis 71,35 (9%)
Each
Farbe:
Tiefrot
Marker oder Farbstoff:
Alexa Fluor™ 647
Preis (EUR)
720,65
Online Exclusive
792,00Ersparnis 71,35 (9%)
Each
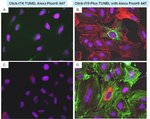
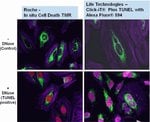
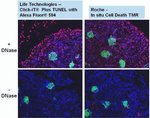
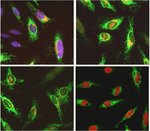
Mit dem Click-iT Plus TUNEL-Assay für den In Situ-Apoptosenachweis, der Alexa Fluor 488, 594 und 647 fluoreszierende Farbstoffoptionen bietet, können Sie mehr apoptotische Zellen in Gewebe- und Zellkulturproben nachweisen. Dieses In-situ-Apoptose-Nachweiskit ist für Gewebe- oder Zellproben optimiert und ermöglicht das Multiplexing der Farbstoffe mit anderen Farbstoffen oder Proteinen, wie GFP und RFP, und lassen sich aufgrund ihrer kleineren Größe (im Vergleich zu Antikörpern) leichter in komplexe Moleküle integrieren. Dieses TUNEL-Assay-Kit ist ebenfalls sehr flexibel und zum Testen von 1 bis 50 Proben in einem einzigen Experiment verwendbar.
Click-iT Plus TUNEL Alexa Fluor 488, 594 und 647 Assays für den In-situ-Apoptosenachweis können apoptotische Zellen in Gewebe- und Zellkulturproben nachweisen, indem sie eine kleine, hochgradig spezifische Markierung und einen hellen Fluoreszenzfarbstoff einarbeiten. Nach Einarbeitung des Markierungsanteils in DNA-Fragmente erfolgt der Nachweis über eine katalysierte „Klick“-Reaktion unter Bedingungen, die das emittierte Fluoreszenzsignal von GFP oder RFP erhalten.
Weitere Vorteile des Click-iT Plus TUNEL-Assays für den In-Situ-Apoptosenachweis:
• Optimiert für den Nachweis apoptotischer Zellen in Gewebe- oder Zellproben
• Multiplex-fähig: Optimiert für die Arbeit mit fluoreszierenden Farbstoffen oder Proteinen wie GFP und RFP
• Verbesserter TUNEL-Assay: Besserer Einbau der Markierung dank eines kleinen reaktiven Anteils
• Helle apoptotische Signale: nutzt Alexa Fluor Farbstoffe, die ein stabiles Fluoreszenzsignal ohne Photobleichung erzeugen
• Flexibilität: Assay ist für gleichzeitige Tests von 1 bis 50 Proben verwendbar
Fragmentierung der zellulären DNA ist ein Kennzeichen von Apoptose. Der TUNEL-Assay ist die am weitesten verbreitete Methode zum Nachweis fragmentierter DNA in apoptotischen Zell- oder Gewebeproben. Der TUNEL-Assay beginnt durch den Einbau modifizierter dUTP am 3'-OH Ende der fragmentierten DNA. Die dUTP-Modifikation besteht oftmals in der Kopplung eines Fluorophors. Aufgrund der Größe des Fluorophors kann das modifizierte dUTP niedrigere als erwartete Einarbeitungsraten aufweisen, was sich auf die Empfindlichkeit des TUNEL-Assays auswirken kann. Zudem weisen viele der in derzeit verfügbaren TUNEL-Assay-Kits enthaltenen Fluorophore Probleme mit Photobleichung und Fluoreszenzspektralüberlappungen auf, die beide die Empfindlichkeit und Multiplex-Möglichkeiten des Assays einschränken.
Der Click-iT Plus TUNEL-Assay soll diese Probleme umgehen. Der Assay verwendet dUTP, modifiziert mit einer Alkingruppe (eine kleine bioorthogonale funktionelle Gruppe), wodurch die Nukleotide leichter aufgenommen werden. Nach dem Einbau führt eine hochgradig spezifische „Klick“-Reaktion zwischen der Alkingruppe und einem Alexa Fluor Picolylazid-Fluoreszenzfarbstoff mit anschließendem Nachweis dieses Farbstoffs zu einem empfindlichen und spezifischen Assay für die Erkennung apoptotischer Zellen oder Gewebeproben. Aufgrund der schonenden Reaktionsbedingungen ermöglicht der Click-iT Plus TUNEL-Assay das Multiplexing mit fluoreszierenden Proteinen oder Farbstoffen.
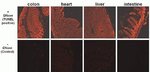
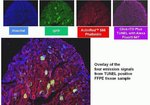
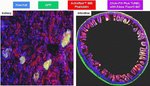
Der Click-iT Plus TUNEL-Assay wurde validiert mit mehreren verschiedenen Formalin-fixierten, Paraffin-eingebetteten Gewebetypen. In allen Fällen ist das Multiplexing mit fluoreszierenden Proteinen und Farbstoffen möglich. Auch die Aktinfärbung mit fluoreszenzmarkiertem Phalloidin ist möglich.
Der Click-iT Plus TUNEL-Assay enthält alle erforderlichen Reagenzien zum Nachweis apoptotischer Zellen in Gewebe- oder Zellproben. Die Reagenzien in diesem Kit reichen zum Testen von 50 Proben und können für die gleichzeitige Analyse von 1 bis 50 Proben verwendet werden.
Weitere Vorteile des Click-iT Plus TUNEL-Assays für den In-Situ-Apoptosenachweis:
• Optimiert für den Nachweis apoptotischer Zellen in Gewebe- oder Zellproben
• Multiplex-fähig: Optimiert für die Arbeit mit fluoreszierenden Farbstoffen oder Proteinen wie GFP und RFP
• Verbesserter TUNEL-Assay: Besserer Einbau der Markierung dank eines kleinen reaktiven Anteils
• Helle apoptotische Signale: nutzt Alexa Fluor Farbstoffe, die ein stabiles Fluoreszenzsignal ohne Photobleichung erzeugen
• Flexibilität: Assay ist für gleichzeitige Tests von 1 bis 50 Proben verwendbar
Fragmentierung der zellulären DNA ist ein Kennzeichen von Apoptose. Der TUNEL-Assay ist die am weitesten verbreitete Methode zum Nachweis fragmentierter DNA in apoptotischen Zell- oder Gewebeproben. Der TUNEL-Assay beginnt durch den Einbau modifizierter dUTP am 3'-OH Ende der fragmentierten DNA. Die dUTP-Modifikation besteht oftmals in der Kopplung eines Fluorophors. Aufgrund der Größe des Fluorophors kann das modifizierte dUTP niedrigere als erwartete Einarbeitungsraten aufweisen, was sich auf die Empfindlichkeit des TUNEL-Assays auswirken kann. Zudem weisen viele der in derzeit verfügbaren TUNEL-Assay-Kits enthaltenen Fluorophore Probleme mit Photobleichung und Fluoreszenzspektralüberlappungen auf, die beide die Empfindlichkeit und Multiplex-Möglichkeiten des Assays einschränken.
Der Click-iT Plus TUNEL-Assay soll diese Probleme umgehen. Der Assay verwendet dUTP, modifiziert mit einer Alkingruppe (eine kleine bioorthogonale funktionelle Gruppe), wodurch die Nukleotide leichter aufgenommen werden. Nach dem Einbau führt eine hochgradig spezifische „Klick“-Reaktion zwischen der Alkingruppe und einem Alexa Fluor Picolylazid-Fluoreszenzfarbstoff mit anschließendem Nachweis dieses Farbstoffs zu einem empfindlichen und spezifischen Assay für die Erkennung apoptotischer Zellen oder Gewebeproben. Aufgrund der schonenden Reaktionsbedingungen ermöglicht der Click-iT Plus TUNEL-Assay das Multiplexing mit fluoreszierenden Proteinen oder Farbstoffen.
Der Click-iT Plus TUNEL-Assay wurde validiert mit mehreren verschiedenen Formalin-fixierten, Paraffin-eingebetteten Gewebetypen. In allen Fällen ist das Multiplexing mit fluoreszierenden Proteinen und Farbstoffen möglich. Auch die Aktinfärbung mit fluoreszenzmarkiertem Phalloidin ist möglich.
Der Click-iT Plus TUNEL-Assay enthält alle erforderlichen Reagenzien zum Nachweis apoptotischer Zellen in Gewebe- oder Zellproben. Die Reagenzien in diesem Kit reichen zum Testen von 50 Proben und können für die gleichzeitige Analyse von 1 bis 50 Proben verwendet werden.
For Research Use Only. Not for use in diagnostic procedures.
Specifications
FarbeTiefrot
BeschreibungClick-iT Plus TUNEL Assay für den In-Situ-Apoptosenachweis, Alexa Fluor™ 647 Farbstoff
Anregung/Emission650/665
Zur Verwendung mit (Geräte)Fluoreszenzmikroskop
MarkertypAlexa Fluor™ Farbstoffe
Marker oder FarbstoffAlexa Fluor™ 647
Anzahl Reaktionen50 Deckgläser
ProduktlinieClick-iT
ProdukttypTUNEL Assay
Menge1 kit
VersandbedingungTrockeneis
LagerungsbedingungenBei ≤ 20°C lagern und vor Licht schützen.
NachweisverfahrenFluoreszenz
FormatDeckglas
Unit SizeEach
Häufig gestellte Fragen (FAQ)
What is the fluorescence excitation and emission maxima of Alexa Fluor 647 dye?
I will be performing a cell proliferation assay using Click-iT EdU kit. At what point can I stop overnight, or do I have to perform all the steps continuously?
I need to test cells for apoptosis after they have been formaldehyde-fixed and permeabilized. What dye or conjugate do you recommend? Will Annexin V conjugates work?
Can I use Click-iT Plus TUNEL Assay Kits for In Situ Apoptosis Detection (Cat. Nos. C10617, C10618, C10619) for whole mount immunofluorescence staining of zebrafish larvae?
I am observing no signal or very low specific signal for my click-labeled samples. What can I do to improve the signal?
Zitierungen und Referenzen (8)
Zitierungen und Referenzen
Abstract
Spontaneous calcium waves in the developing enteric nervous system.
Journal:Dev Biol
PubMed ID:28528728
The enteric nervous system (ENS) is an extensive network of neurons in the gut wall that arises from neural crest-derived cells. Like other populations of neural crest cells, it is known that enteric neural crest-derived cells (ENCCs) influence the behaviour of each other and therefore must communicate. However, little is
Arundic Acid Prevents Developmental Upregulation of S100B Expression and Inhibits Enteric Glial Development.
Journal:Front Cell Neurosci
PubMed ID:28280459
S100B is expressed in various types of glial cells and is involved in regulating many aspects of their function. However, little is known about its role during nervous system development. In this study, we investigated the effect of inhibiting the onset of S100B synthesis in the development of the enteric
The impact of detergents on the tissue decellularization process: A ToF-SIMS study.
Journal:Acta Biomater
PubMed ID:27993639
Biologic scaffolds are derived from mammalian tissues, which must be decellularized to remove cellular antigens that would otherwise incite an adverse immune response. Although widely used clinically, the optimum balance between cell removal and the disruption of matrix architecture and surface ligand landscape remains a considerable challenge. Here we describe
Angiopoietin-1 deficiency increases renal capillary rarefaction and tubulointerstitial fibrosis in mice.
Journal:PLoS One
PubMed ID:29293543
Presence of tubulointerstitial fibrosis is predictive of progressive decline in kidney function, independent of its underlying cause. Injury to the renal microvasculature is a major factor in the progression of fibrosis and identification of factors that regulate endothelium in fibrosis is desirable as they might be candidate targets for treatment
Dual roles of hydrogen peroxide in promoting zebrafish renal repair and regeneration.
Journal:Biochem Biophys Res Commun
PubMed ID:31248596
Acute renal injury (AKI) is a serious disorder of renal failure or renal damage that occurs within hours or days. At present, there is no approved pharmaceutical treatment for AKI. Zebrafish is an excellent model for studying the repair of AKI because of its remarkable ability to repair kidney injury.