Search Thermo Fisher Scientific
Thermo Scientific™
Pierce™ Glutathione Chromatography Cartridges, 1 mL
Référence: 16109
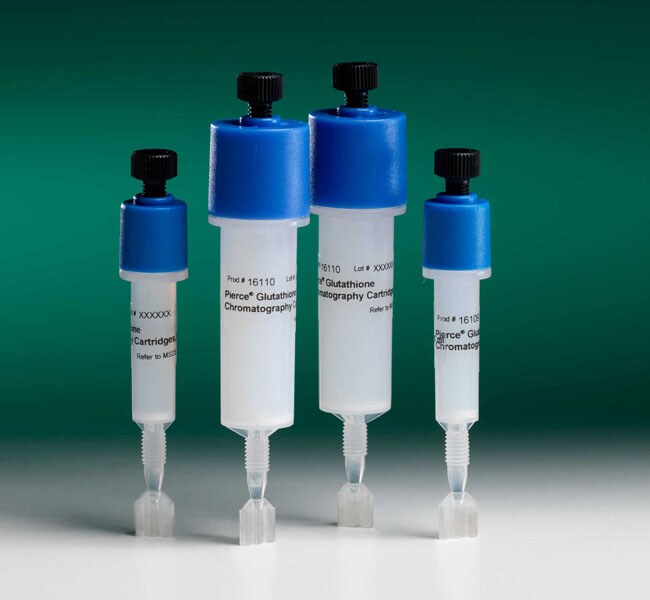
Thermo Scientific™
Pierce™ Glutathione Chromatography Cartridges, 1 mL
Référence: 16109
Référence
16109
Taille de l’unité
5 x 1 mL
Prix (EUR)
Prix 372,00
Votre prix
Disponibilité
-
Quantité
Quantité
| Référence | Taille de l’unité | Prix (EUR) | Disponibilité | Quantité | |
|---|---|---|---|---|---|
| 16109 | 5 x 1 mL | Prix 372,00 Votre prix | - | ||
| 16110 | 2 x 5 mL | Prix 646,00 Votre prix | - |
Présentation du produit
Figures
Vidéos
Recommandations
Recommandations
Documentation
Foire aux questions
Citations et références
Informations supplémentaires
Recommandations
Les cartouches de chromatographie Glutathion Pierce Thermo Scientific sont des dispositifs préemballés pratiques et prêts à l’emploi pour la purification des protéines de fusion GST à partir de lysats cellulaires.
Caractéristiques du gluthalion-agarose :
• Haute capacité —lie au moins 40 mg de protéine GST recombinante purifiée par millilitre de résine
• Rendement élevé et pureté — purifie de façon uniforme au moins 10 mg de protéine marquée GST par millilitre de résine avec une pureté supérieure à 90 %
• Économique — la résine est proposée à un prix économique et peut être réutilisée au minimum cinq fois sans aucune réduction de la capacité de liaison et des performances de la purification
• Polyvalent — performant pour purifier les protéines de fusion GST à partir de lysats bactériens ou pour une utilisation avec des protéines marquées à la GST pré-purifiées afin de réduire les interactions de protéines
• Compatible — validée et efficace pour une utilisation avec les réactifs de lyse cellulaire Thermo Scientific pour extraire et purifier à partir de cultures de cellules de mammifères ou de bactéries
Le glutathion est immobilisé par son sulfhydryle central sur une résine d’agarose réticulée à 6 %. La purification de protéines hybrides “taguées” au GST avec du glutathion (GSH) sur des billes d’agarose est bien documentée et fournit une purification par affinité en une étape et d’une pureté élevée. Que ce soit pour purifier de grandes quantités de protéine recombinante de lysats E. coli ou pour analyser des interactions de protéines impliquant des protéines appâts marquées à la GST, la résine de glutathion-agarose convient parfaitement à la tâche.
L’agarose au glutathion Thermo Scientific Pierce est également disponible en trois volumes de pâtes de résine, en kits complets de purification GST, en deux tailles de cartouches de chromatographie prêtes pour le système FPLC et en plaques de filtration à 96 puits pour des besoins de rendement importants.
L’agarose-glutathion Pierce permet de purifier avec une grande efficacité des taux élevés de protéines de fusion surexprimées et marquées par la GSTà partir de lysats bactériens, tels que celles obtenues avec les réactifs Thermo Scientific BPER pour l’extraction des protéines bactériennes.
L’agarose-glutathion Pierce offre des résultats performants pour la fixation par lots et les procédures basées sur des colonnes de centrifugation à de nombreuses échelles. Ses performances sont comparables ou supérieures à celles des résines GSH appréciées d’autres fabricants.
La résine glutathion-agarose Pierce est un support de haute qualité, stable et résistant. Les tests confirment l’absence de toute dégradation des performances de la résine après au moins cinq utilisations consécutives. Ces données indiquent que, dans des conditions normales, la résine offre une grande résistance à la dégradation structurelle, ainsi qu’à l’infiltration de ligand.
L'expression et la purification des protéines recombinantes est essentielle aux études de régulation, structure et fonction des protéines. La majorité des protéines recombinantes sont exprimées sous forme de fusion avec de courts “tags” d’affinité ou de petites protéines, comme le glutathion S-transférase (GST). Cette protéine se lie principalement au glutathion réduit (GSH) dans des conditions quasineutres et non dénaturantes (par exemple tampon Tris). La protéine fixée peut être facilement dissociée (éluée) par déplacement compétitif à l’aide d’un tampon contenant du GSH réduit libre (glutathion oxydé ; le GSSH n’est pas efficace à cet effet). Lorsque les protéines d’intérêt sont exprimées en tant que protéines de fusion à l’aide de GST et que le glutathion est fixé sur un support solide, ce système de protéine substrat rend possible la purification par affinité des protéines recombinantes, ainsi que d’autres expériences sur ces protéines.
Produits associés
Pierce™ Cartouches de chromatographie glutathion, 1 ml
Pierce™ Colonnes de centrifugation Glutathion, 3 ml
Pierce™ Glutathion-agarose
Caractéristiques du gluthalion-agarose :
• Haute capacité —lie au moins 40 mg de protéine GST recombinante purifiée par millilitre de résine
• Rendement élevé et pureté — purifie de façon uniforme au moins 10 mg de protéine marquée GST par millilitre de résine avec une pureté supérieure à 90 %
• Économique — la résine est proposée à un prix économique et peut être réutilisée au minimum cinq fois sans aucune réduction de la capacité de liaison et des performances de la purification
• Polyvalent — performant pour purifier les protéines de fusion GST à partir de lysats bactériens ou pour une utilisation avec des protéines marquées à la GST pré-purifiées afin de réduire les interactions de protéines
• Compatible — validée et efficace pour une utilisation avec les réactifs de lyse cellulaire Thermo Scientific pour extraire et purifier à partir de cultures de cellules de mammifères ou de bactéries
Le glutathion est immobilisé par son sulfhydryle central sur une résine d’agarose réticulée à 6 %. La purification de protéines hybrides “taguées” au GST avec du glutathion (GSH) sur des billes d’agarose est bien documentée et fournit une purification par affinité en une étape et d’une pureté élevée. Que ce soit pour purifier de grandes quantités de protéine recombinante de lysats E. coli ou pour analyser des interactions de protéines impliquant des protéines appâts marquées à la GST, la résine de glutathion-agarose convient parfaitement à la tâche.
L’agarose au glutathion Thermo Scientific Pierce est également disponible en trois volumes de pâtes de résine, en kits complets de purification GST, en deux tailles de cartouches de chromatographie prêtes pour le système FPLC et en plaques de filtration à 96 puits pour des besoins de rendement importants.
L’agarose-glutathion Pierce permet de purifier avec une grande efficacité des taux élevés de protéines de fusion surexprimées et marquées par la GSTà partir de lysats bactériens, tels que celles obtenues avec les réactifs Thermo Scientific BPER pour l’extraction des protéines bactériennes.
L’agarose-glutathion Pierce offre des résultats performants pour la fixation par lots et les procédures basées sur des colonnes de centrifugation à de nombreuses échelles. Ses performances sont comparables ou supérieures à celles des résines GSH appréciées d’autres fabricants.
La résine glutathion-agarose Pierce est un support de haute qualité, stable et résistant. Les tests confirment l’absence de toute dégradation des performances de la résine après au moins cinq utilisations consécutives. Ces données indiquent que, dans des conditions normales, la résine offre une grande résistance à la dégradation structurelle, ainsi qu’à l’infiltration de ligand.
L'expression et la purification des protéines recombinantes est essentielle aux études de régulation, structure et fonction des protéines. La majorité des protéines recombinantes sont exprimées sous forme de fusion avec de courts “tags” d’affinité ou de petites protéines, comme le glutathion S-transférase (GST). Cette protéine se lie principalement au glutathion réduit (GSH) dans des conditions quasineutres et non dénaturantes (par exemple tampon Tris). La protéine fixée peut être facilement dissociée (éluée) par déplacement compétitif à l’aide d’un tampon contenant du GSH réduit libre (glutathion oxydé ; le GSSH n’est pas efficace à cet effet). Lorsque les protéines d’intérêt sont exprimées en tant que protéines de fusion à l’aide de GST et que le glutathion est fixé sur un support solide, ce système de protéine substrat rend possible la purification par affinité des protéines recombinantes, ainsi que d’autres expériences sur ces protéines.
Produits associés
Pierce™ Cartouches de chromatographie glutathion, 1 ml
Pierce™ Colonnes de centrifugation Glutathion, 3 ml
Pierce™ Glutathion-agarose
For Research Use Only. Not for use in diagnostic procedures.
Spécifications
Capacité (métrique)
1 ml
Description
Cartouches de chromatographie glutathion Pierce, 1 ml
Forme
Liquide
Gamme de produits
Pierce™
Quantité
5 cartouches
Forme protéique
Recombinant
Cible
Protéine marquée à la GST
Type
Cartouche de chromatographie
Phase stationnaire
Glutathion
Type de colonne
Affinité, résine d’agarose
Contenu et stockage
Dès réception, stocker entre 4 à 8°C. Ne pas congeler.
Figures
Documentation et téléchargements
Certificats
Recherchez par numéro de lot ou numéro de lot partiel
Foire aux questions (FAQ)
Citations et références
Search citations by name, author, journal title or abstract text