多能性幹細胞とは?
ヒト多能性幹細胞(PSC)は、自己を際限なく再生し、適切な微小環境においてヒト体内に存在するほぼ全ての細胞タイプに分化する能力を特徴とします。PSCは、胚性幹細胞(ESC)と人工多能性幹細胞(iPSC)の2種類が一般的に研究されています(図2.1)。ヒトESCは、発生中の胚の胚盤胞期の内部細胞塊から単離されます*1 。iPSCは、ESCと同等または類似する細胞ですが、成体体細胞をリプログラミングするためのOCT3/4、KLF4、SOX2、およびc-MYCなどのリプログラミング因子の発現を経て生成します*2,3 。iPSCは、患者の幹細胞の誘導を簡素化することにより幹細胞研究に革命をもたらしました。これにより、iPSCを使用して、シャーレ中で疾患特異的な細胞タイプのモデルを作製することが可能となりました。これらのモデルは、疾患病態のメカニズムを定義するのに有用で、治療ターゲットの同定や創薬において重要な役割を果たすことができます。機能的な成熟細胞に分化するよう方向付けることが可能なiPSCを無制限に供給できることは、糖尿病、肝疾患、およびパーキンソン病やアルツハイマー病などの様々な疾患に対する細胞療法のための原材料として非常に有望視されています。

多能性幹細胞のキャラクタリゼーション
iPSCおよびESCでは、未分化幹細胞状態を維持するためにNanogおよびOCT4などのキー転写因子の発現が必要とされます*4 。これらの転写因子は、細胞の分裂、分化、および発達に重要な遺伝子を調節します。これらの転写因子の他に、TRA-1-60、TRA-1-81、SSEA3、およびSSEA4などの特定の一連の細胞表面タンパク質は、通常、PSCによって発現します。これらのマーカーの存在の検出は、新たに誘導されたiPSC株(iPSC line)およびESC株(ES Cline)のキャラクタリゼーションにおける最初のステップの1つです。特定の細胞の染色は、これらの確立された多能性マーカーに対する抗体を使用することで達成できます(表2.1)。
生細胞の免疫染色
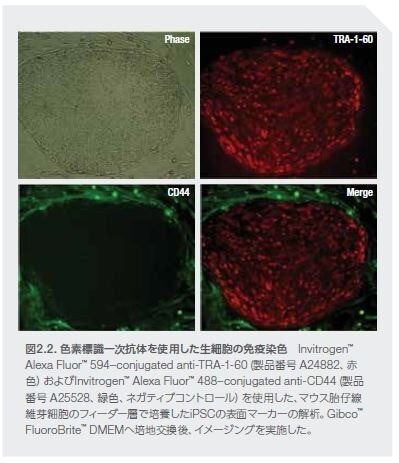
細胞表面タンパク質は、全細胞に色素標識抗体で迅速に染色することができます。放射線照射したマウス胎仔線維芽細胞(MEF)のフィーダー層上で培養したiPSCコロニー上のPSC表面マーカーTRA-1-60の生細胞免疫染色の例を図2.2に示します。CD44は、MEFを含む多くの分化細胞で発現される表面タンパク質ですが、PSCでは発現しません。新たに誘導したiPSCコロニーが完全にリプログラミングされているかの確認には、TRA-1-60のポジティブ染色とCD44のネガティブ染色を使用することができます。
固定細胞の免疫染色
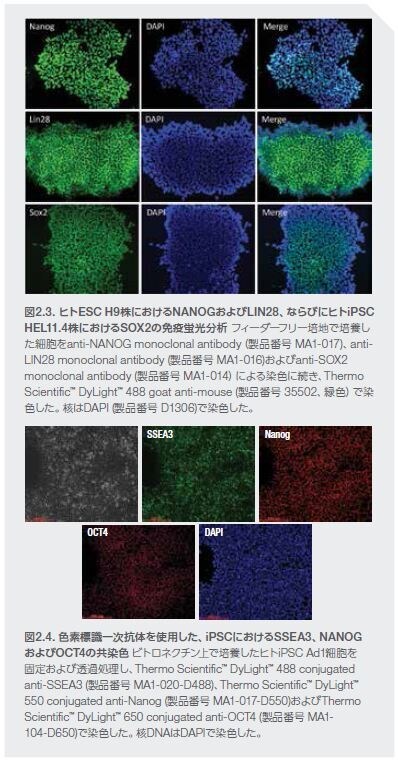
iPSCクローンの品質の信頼性を向上させるためには、わずか1つか2つでなく、複数のPSCマーカーの発現について確認することが推奨されます。Oct4、Nanog、Lin28、およびSox2などの一部のマーカーは細胞内タンパク質であるため、これらのマーカーの染色を行う際は固定および透過処理が必要とされます(図2.3)。これらのマーカーおよび他のPSCマーカーに対する色素標識一次抗体を使用すると(表2.1)、二次抗体染色工程を回避でき、実験にかかる時間とコストを削減し、多重染色を行うことが可能です(図2.4)。
フローサイトメトリー
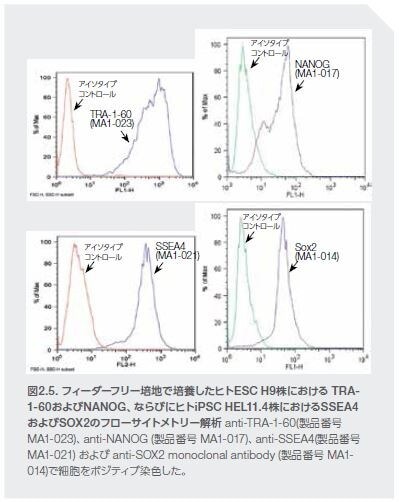
上述の染色およびイメージングのアプローチは定性的であるのに対し、フローサイトメトリーはマーカーを発現した細胞の個数およびその蛍光強度の定量的測定を提供し、マーカーのあらゆるダウンレギュレーション、あるいは細胞集団の不均一性を明らかにします。最も一般的なのは、SSEA4およびTRA-1-60などの表面マーカーを使用するフローサイトメトリーですが、固定および透過処理した細胞を使用して、NanogおよびSOX2などの核マーカーを使用するフローサイトメトリーを実施することも可能です(図2.5)。
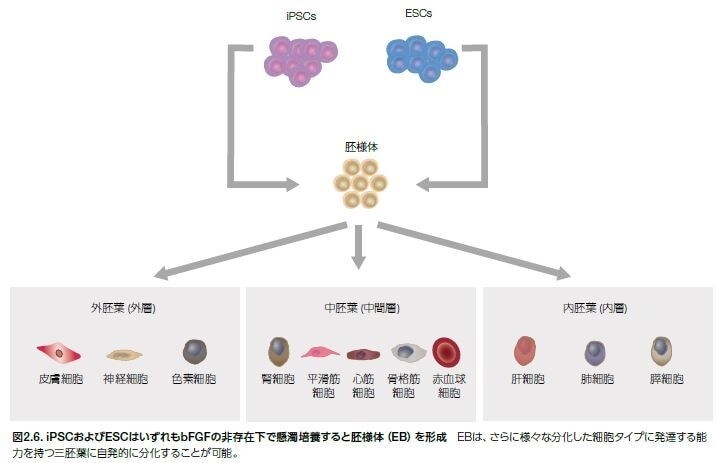
PSCの解析および自己複製遺伝子産物の存在や体細胞遺伝子産物の不在について確認することは重要ですが、PSC株の機能的多能性についての確認には十分ではありません。この他の重要な試験に、PSCの三胚葉(外胚葉、中胚葉、内胚葉)の各細胞への分化能の評価があります(図2.6)。この試験は、 in vitro および in vitroのいずれのアプローチによっても達成できます。
テラトーマ形成
マウスPSCを使用する場合、四倍体補完法、キメラ作製、および生殖系列伝達などの数多くの in vitro アッセイを通して、分化能を評価することができます。これらはヒト細胞で実行可能な選択肢ではないため、代わりにヒトPSCをマウスに注入し、テラトーマを形成させて、三胚葉への分化能を確認することで解析することが可能です。in vitro アッセイでは、生理的条件下での細胞の分化が可能なため、テラトーマ形成はPSCの分化能を確認するためのゴールドスタンダードと考えられます。しかしながら、この方法は非常に手間がかかり、完了まで6~12週間を要し、動物実験の負担が大きいことから、常に実施されるわけではありません。
胚様体(EB)形成
テラトーマ形成に代わるより一般的な方法は、EB形成という in vitro アッセイで、7~21日でPSCが三胚葉に自発的に分化します。分化は非生理的条件下で生じますが、EB形成はより迅速で、労力が少なく、簡単に解析できるという利点があります。EBにおける分化を解析するための一般的なマーカーには、中胚葉の平滑筋アクチン(SMA)、内胚葉の初期肝細胞マーカーのα-フェトプロテイン(AFP)、および外胚葉のニューロンマーカーのβ-IIIチューブリン(TUBB3)があります(図2.7)。一連の胚葉マーカーを使用する免疫蛍光は、これらの各マーカーが特定の細胞系統で選択的に発現するだけでなく、視認による追加の測定として機能し細胞内局在パターンの識別も示す点で特に有用です。例えば、抗TUBB3染色は、特徴的なニューロン様突起を持つ細長い細胞に対する一般的に最も明るい染色です。SMAをしっかり発現する細胞では、アクチンフィラメント染色の線模様が表示されます。これらの細胞は、大きい層のグループによく見られ、時には鰓状の形状を持つ大型細胞として単離されます。抗AFP染色は、通常、それぞれ核の周囲にリング状と呼ばれる染色パターンを持つ細胞の密集したクラスターを同定します。他にも多くのマーカー、例えば、内胚葉のPDX1およびSox17、外胚葉のSox1およびOtx2、ならびに中胚葉のNKX2.5およびPDGFRaが各胚葉のキャラクタリゼーションに使用されてきています(表2.2)。

参考文献:
1. Thomson JA, Itskovitz-Eldor J, Shapiro SS et al. (1998) Embryonic stem cell lines derived from human blastocysts. Science 282(5391):1145–1147.
2. Takahashi K, Yamanaka S (2006) Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors. Cell 126(4):663–676.
3. Yu J, Vodyanik MA, Smuga-Otto K et al. (2007) Induced pluripotent stem cell lines derived from human somatic cells. Science 318(5858):1917–1920.
4. Pan GJ, Thomson JA (2007) Nanog and transcriptional networks in embryonic stem cell pluripotency. Cell Res 17(1):42–49.
【無料ダウンロード】幹細胞研究用抗体ガイドブック
本ガイドブックでは、幹細胞研究に関する深い知識の習得、および最新の研究に役立つ抗体関連製品の情報を提供しております。
研究用にのみ使用できます。診断用には使用いただけません。



