2021年1月~3月に開催した「やってみたシリーズ アイデア募集イベント」に多くのご応募をいただきありがとうございました!皆さまから頂いたアイデアについて社内で検討し、Blogの記事として公開するテーマを決定し、これまでに2つの記事をご報告しました。今回はROX補正について追加の「やってみた実験」が完了したので、その結果を公開します。
既に公開した、トランスフェクション試薬のインキュベーション時間についての記事はこちら、前回のピペッティング誤差についてのROX補正の記事はこちらをご覧ください。
はじめに
今回も前回に引き続き、ハンドルネーム “Narupiyo” さんからご応募いただいたアイデアです。
「リアルタイムPCR ROXはどこまで誤差を補正してくれるのか検証してみた」 どの程度までピペッティング誤差を補正してくれているのでしょうか.(原文まま)。
前回は、±10 µL というかなりおおきなピペッティング誤差をROX補正してみました。リアルタイムPCRでのウェル間のばらつきはピペッティング誤差だけでなく、反応液の飛散・反応液中の気泡・プレート表面の汚れ、などさまざまな要因が考えられます。“Narupiyo” さんからROX補正についてのアイデアをご応募いただきましたので、さまざまな要因によるウェル間のばらつきをROXで補正できるのか試していくことにしました!まず初めに、反応液の飛散がデータに与える影響とROX補正の効果を検証します。
ちなみにROX補正とは、反応液中に含まれているリファレンスとなるROX色素の蛍光強度で、レポーター色素(e.g. FAM, VICまたはSYBR™ Green)の蛍光強度を割ることにより、ウェル間のばらつきを標準化することです。ROX補正について動画もご用意しておりますので、ぜひご覧ください!
材料と方法
材料:
| リアルタイムPCR反応液 | (μL) |
| HeLa cDNA(1 ng/µL) | 2 |
| TaqMan™ Fast Advanced Master Mix | 10 |
| TaqMan Gene Expression Assay (20x) GAPDH | 1 |
| Nuclease-Free Water | 7 |
| Total | 20 |
※ウェル 間で調製誤差が生じないようにするため必要本数分まとめて調製し、各容量を分注しました。
方法:
各ウェルに20 µLの反応液を分注し、タッピングにより反応液をチューブ内に飛散させました(図1)。これを飛び散り処理区と呼ぶことにします。前回と同様、リアルタイムPCRシステムは、Applied Biosystems™ QuantStudio™ 5 Real-Time PCR Systemを使用し、Fast モードに設定して下記条件でランを実施しました。
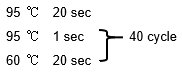
反応液を飛散させないコントロールと飛び散り処理区について、増幅曲線とCT値を比較しました(n = 5)。

結果と考察
それでは、反応液をわざと激しめに飛び散らせた場合のリアルタイムPCR実験の結果をご報告します。PCR反応後にチューブを回収し目視で確認したところ、コントロールと比較して飛び散り処理区では反応液が飛び散ったままでした(図2)。また、飛び散りの影響なのかチューブ内の壁面が結露していることがはっきり認識できました。

まず、ROX補正をしない場合の結果を確認しましょう。コントロールと比較して、飛び散り処理区ではウェル間のばらつきが大きい結果となりました(図3上)。これは、5つのウェルそれぞれで飛び散り方が異なることに起因するばらつきであると考えられます。また、飛び散り処理区のCT値が高いのは(図4)、反応液が飛び散ることで反応液量が少ない条件と同じような状況になっていると推察されます。前回、反応液量10, 20, 30 µLを比較した【やってみた】記事はこちらからご覧いただけます。
次に、ROX補正した場合の結果を確認しましょう。ぱっと見ると赤い線が1本だけあるように見え、きちんとROXで補正できたことが分かります(図3下)。実際はn = 5 の実験なので、コントロールが5本、飛び散り処理区が5本、合計10本の線が描かれていますが、ほぼ完全に重なっているので1本のように見えます。

CT値を確認してみると、ROX補正なしの飛び散り処理区はばらつきが大きかったのですが、ROX補正をすることによりばらつきを小さくすることができました(図4)。さらに、コントロールと飛び散り処理区のCT値も同程度の値になり、ROX補正により反応液の飛び散りによる誤差を小さくでき、精度の高い定量値を得られることが分かりました。

まとめ
いかがでしたでしょうか。
今回の実験では、PCR反応液をタッピングにより激しめに飛び散らせ、わざとスピンダウンせずにそのままリアルタイムPCRを実施してみました。その結果、反応液の飛び散りについてもきちんとROXで補正できることをお示しできました。しかし、皆さまがリアルタイムPCRを実施される際にはROX補正を過信されることなく、反応液が飛び散っていてもいなくても念のためスピンダウンしてから反応を開始することをおすすめしております。
今回の実験も、2021年1月~3月に開催した「やってみたシリーズ アイデア募集イベント」にご応募いただいたアイデアにお応えするかたちで実施しました。元のアイデアは “Narupiyo” さんからご応募いただいたもので、もう少しROX補正についてのやってみた実験をやってみる予定です。“Narupiyo” さんアイデアをご応募いただきありがとうございました!
弊社ではRNA抽出やリアルタイムPCR、他にも細胞培養、ウェスタンブロッティングなど、実際に実験(実習)を行いつつ学べる各種ハンズオントレーニングを開催しています。その中で今回のような実験結果もご紹介していますので、これから新しい実験を始められる方、より理解を深めたい方はぜひご参加ください!
今回の記事に関連する、過去のBlog:
【やってみた】トランスフェクション前の試薬のインキュベーション時間、0~24時間までふってみた
【やってみた】リアルタイムPCRの反応液分注ピペッティング誤差をROX補正してみた
リアルタイムPCR実験で陥りがちな落とし穴Top10
「CT値」「解離曲線」って何? リアルタイムPCR解析で用いられる用語まとめ
蛍光シグナルに変動を起こす原因とは? リアルタイムPCRにおける光学的変動
これでもう失敗しない!リアルタイムPCRに失敗する4つの問題点と解決策をご紹介
リアルタイムPCRハンドブック 無料ダウンロード
このハンドブックでは、リアルタイムPCRの理論や実験デザインの設計など、リアルタイムPCRの基礎知識が掲載されています。リアルタイムPCRを始めたばかりの方やこれから実験を考えている方にうってつけのハンドブックです。PDFファイルのダウンロードをご希望の方は、下記ボタンよりお申し込みください。
リアルタイムPCRトラブルシューティング 無料ダウンロード
異常なS字状の増幅曲線、NTCでの増幅検出、増幅が見られないなど、リアルタイムPCRの実験中に困った際の手助けになる情報を紹介しています。PDFファイルのダウンロードをご希望の方は、下記ボタンよりお申し込みください。
研究用にのみ使用できます。診断用には使用いただけません。



